-
0
Patient Assessment
- 0.1 Patient demand
- 0.2 Overarching considerations
- 0.3 Local history
- 0.4 Anatomical location
- 0.5 General patient history
-
0.6
Risk assessment & special high risk categories
- 5.1 Risk assessment & special high risk categories
- 5.2 age
- 5.3 Compliance
- 5.4 Smoking
- 5.5 Drug abuse
- 5.6 Recreational drugs and alcohol abuse
- 5.7 Parafunctions
- 5.8 Diabetes
- 5.9 Osteoporosis
- 5.10 Coagulation disorders and anticoagulant therapy
- 5.11 Steroids
- 5.12 Bisphosphonates
- 5.13 BRONJ / ARONJ
- 5.14 Radiotherapy
- 5.15 Risk factors
-
1
Diagnostics
-
1.1
Clinical Assessment
- 0.1 Lip line
- 0.2 Mouth opening
- 0.3 Vertical dimension
- 0.4 Maxillo-mandibular relationship
- 0.5 TMD
- 0.6 Existing prosthesis
- 0.7 Muco-gingival junction
- 0.8 Hyposalivation and Xerostomia
- 1.2 Clinical findings
-
1.3
Clinical diagnostic assessments
- 2.1 Microbiology
- 2.2 Salivary output
-
1.4
Diagnostic imaging
- 3.1 Imaging overview
- 3.2 Intraoral radiographs
- 3.3 Panoramic
- 3.4 CBCT
- 3.5 CT
- 1.5 Diagnostic prosthodontic guides
-
1.1
Clinical Assessment
-
2
Treatment Options
- 2.1 Mucosally-supported
-
2.2
Implant-retained/supported, general
- 1.1 Prosthodontic options overview
- 1.2 Number of implants maxilla and mandible
- 1.3 Time to function
- 1.4 Submerged or non-submerged
- 1.5 Soft tissue management
- 1.6 Hard tissue management, mandible
- 1.7 Hard tissue management, maxilla
- 1.8 Need for grafting
- 1.9 Healed vs fresh extraction socket
- 1.10 Digital treatment planning protocols
- 2.3 Implant prosthetics - removable
-
2.4
Implant prosthetics - fixed
- 2.5 Comprehensive treatment concepts
-
3
Treatment Procedures
-
3.1
Surgical
-
3.2
Removable prosthetics
-
3.3
Fixed prosthetics
-
3.1
Surgical
- 4 Aftercare
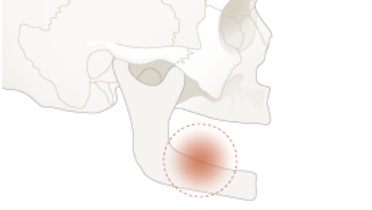
感染症 – 微生物学的診断
Key points
- 辺縁骨吸収はポケットの深化を引き起こします。菌交代現象がインプラント周囲炎を引き起こすこともあります。
- インプラント周囲炎の場合は、微生物感受性試験が臨床的に重要であり、これを裏付けるエビデンスもあります。
微生物叢パラメータ
インプラントの存在または本数は、無歯顎患者の唾液中および舌上の好気性および嫌気性菌種に影響を与えます。
インプラント周囲炎に認められる歯肉縁下生物叢は、試験によって差があります。部分無歯顎患者は、歯周病原菌が少ないことが報告されています。Prevotella nigrescens、Fusobacterium nucleatum、P. gingivalis、T. forsythia、Treponema denticolaおよびAggregatibacter actinomycetemcomitansは、インプラント周囲炎を引き起こすことが報告されています。インプラント周囲炎の微生物叢は、ペプトストレプトコッカスまたはブドウ球菌の多い歯周炎とは異なり、腸内桿菌、ブドウ球菌および酵母菌が典型的です。
抗生物質の選択
インプラント周囲炎に関しては、機械的/外科的治療の補助療法としての全身性抗生物質の効果は、未だ確認されていません。粘膜下生物叢の組成が治療有効性の決定因子であるかどうかも未だ明かではありません。微生物試験は、耐性菌種を検出し、適切な抗生物質を選択するのに有効です。
微生物試験
外来患者に行える試験:
- 位相差顕微鏡検査
- 培養
- ラテックス凝集反応
- チェッカーボードDNA-DNAハイブリダイゼーション
- ポリメラーゼ連鎖反応
位相差顕微鏡検査:
球菌/桿菌/糸状菌および運動性細菌の割合を算定する単純かつ迅速なチェアサイド試験。運動性細菌の増加率は歯周炎の侵襲性と関連することが報告されていますが、この関係はインプラント周囲炎では確認されていません。
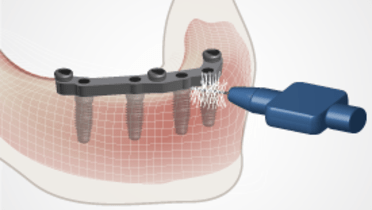
培養
培養はテクニックセンシティブであり、時間もかかりますが、抗生物質に対する感受性を確認することができます。
インプラント周囲のポケットにペーパーポイントを挿入し、バイアルに入れて検査室に移送します。
ラテックス凝集反応
特異抗体でコーティングしたビーズを使用します。サンプルに含まれる標的抗原に接触すると、ビーズの凝集が起こります。単純かつ迅速な検査法です。
チェッカーボードDNA-DNAハイブリダイゼーション
複雑な生態系に最適な試験です。多数のサンプルで多数の菌種を同定することができます。 ≥104の細菌を検出することができます。
ポリメラーゼ連鎖反応
プライマーを用いてDNA排列を増幅させ、増幅が起こると、標的菌種の存在が証明されます。≥ 10の細菌を検出することができます。バイオフィルムに反応を阻害する酵素が含まれていることがあります。